近日,青岛科技大学生物工程学院顾玉超教授团队与中国科学院微生物研究所王为善研究员团队合作,在国际权威期刊《Journal of Controlled Release》(中国科学院一区,Top期刊)在线发表了一项关于癌症免疫治疗的最新研究成果。该研究题为“EngineeringEscherichia coliNissle 1917 to scavenge lactate enhances anti-tumor immunity”(工程化大肠杆菌Nissle 1917清除乳酸增强抗肿瘤免疫)。
该研究首次揭示了乳酸代谢是益生菌大肠杆菌Nissle 1917(EcN)发挥抗肿瘤活性的关键机制,并成功构建了一种具有超强乳酸代谢能力的工程化菌株BELAC。该菌株能高效清除肿瘤微环境中的乳酸,逆转免疫抑制状态,显著激活机体抗肿瘤免疫反应,为开发新一代安全、高效的细菌免疫疗法提供了全新的策略和理论依据。
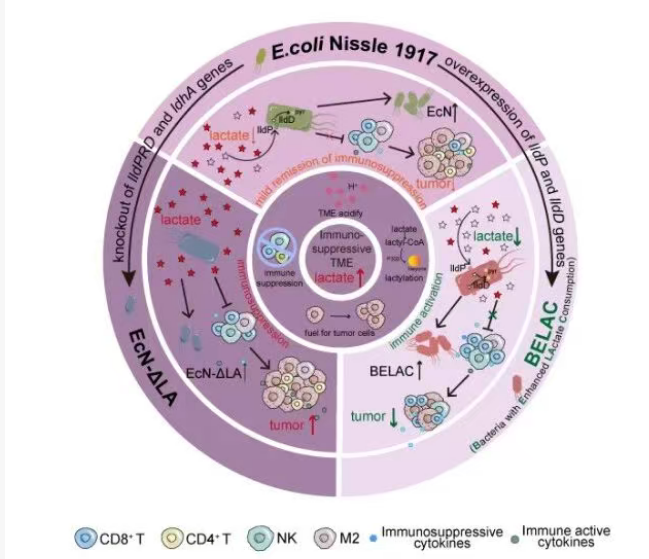
据介绍,肿瘤细胞即使在氧气充足的情况下,也倾向于通过糖酵解进行葡萄糖代谢,同时产生大量乳酸,这一现象被称为“瓦博格效应”。高浓度的乳酸不仅酸化肿瘤微环境,还是一种强效的免疫抑制分子,它能直接抑制杀伤性T细胞的功能,促进免疫抑制细胞的聚集,从而帮助肿瘤细胞逃避免疫系统的攻击。
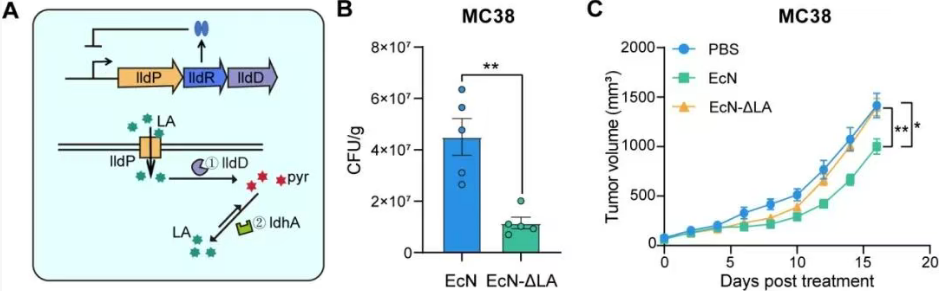
团队采用基因组整合策略,将强化后的乳酸代谢基因盒稳定整合到EcN染色体中,成功构建了一株无质粒、基因组稳定、具有超强乳酸代谢能力的工程菌株,命名为BELAC(Bacteria with Enhanced LActate Consumption)。在B16、MC38和CT26等多种小鼠同源肿瘤模型中,BELAC展现出优异的抗肿瘤效果和安全性。值得注意的是,研究也客观指出,在免疫原性极低的“冷”肿瘤(如4T1乳腺癌)模型中,单靠清除乳酸尚不足以完全抑制肿瘤,这提示未来可将BELAC与免疫检查点抑制剂等疗法联用,以攻克更难治的肿瘤类型。
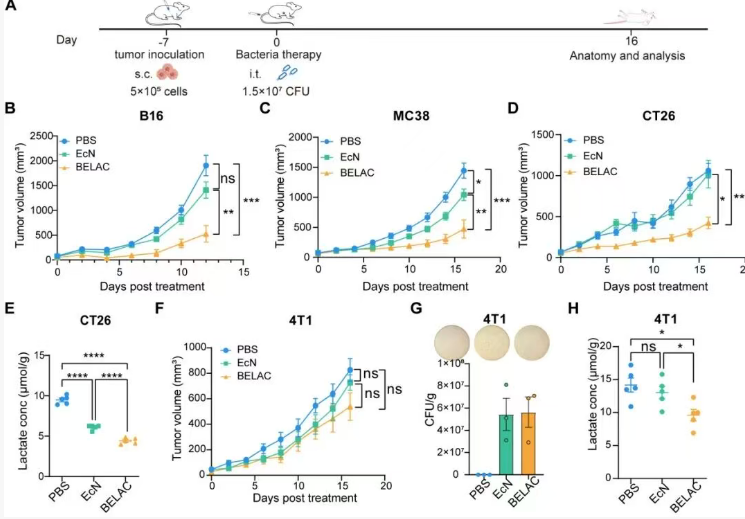
这项研究不仅阐明了EcN抗肿瘤的代谢基础,更通过b增强细菌自身对乳酸的代谢功能实现了对肿瘤微环境的原位、持续调控,从而实现肿瘤免疫抑制微环境的重编程。更重要的是,BELAC菌株具有良好的遗传稳定性和安全性,未来可作为“底盘”细胞,为癌症治疗提供了一种可临床转化的通用平台,进一步联合其他免疫疗法,为癌症患者带来新的希望。
该研究得到了国家自然科学基金、国家重点研发计划、山东省海洋科技基金及泰山学者项目等多项资助。
青岛财经日报/首页新闻记者 国瑾
责任编辑:王海山




请输入验证码